生化学工業の関節機能改善剤「VISCO-3」米国食品医薬品局より承認を取得

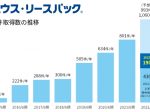
■米国のヒアルロン酸製剤市場は成長を続けており、特に3回投与が売上を伸ばしている
生化学工業<4548>(東1)は25日、関節機能改善剤「VISCO-3(ヴィスコ・スリー)」について、12月21日(米国時間)付で米国食品医薬品局(以下、FDA)より承認を取得したことを発表。
「VISCO-3」は、ヒアルロン酸を主成分とする関節機能改善剤。1治療当たり3回投与する3本キット製品。
米国のヒアルロン酸製剤市場は成長を続けており、特に3回投与が売上を伸ばしていることから、14年3月より「VISCO-3」3回投与の競合製品の非劣性臨床試験を実施し、その結果によりFDAからの承認を新たに取得した。
米国では人口の高齢化に伴い、変形性膝関節症の発生率が増加傾向にあり、今後も関節機能改善剤の市場拡大が予想されている。単回投与製品「Gel-One(R)」、5回投与製品「SUPARTZ FXTM」に加え、3回投与製品「VISCO-3」を新たに市場投入することで、様々なニーズに対応できるよう品揃えを充実させている。