【どう見るこの株】4月高値から調整のアンジェスMGの行方
- 2016/6/27 09:55
- どう見るこの株

■HGF遺伝子治療薬の承認申請へ開発スピードアップ、経費も大幅削減、株価は全般相場落ち着けば急出直りへ
アンジェス MG<4563>(東マ・100株)は世界初のHGF遺伝子治療薬開発を評価して200円前後のモミ合いを2月に上放れて4月20日に943円と急伸した。しかし、信用取引の規制、イギリスのEU離脱による全般相場の急落などが重なって24日には308円まで下げた。去る、6月20日にはHGF遺伝子治療薬の早期実用化を目指して海外における開発戦略変更を発表。また、去る16日には森下仁丹へ子宮頚部前がん治療ワクチンの開発・製造・販売権許諾を発表、一時金とロイヤリティ収入が期待できるが、これら好材料は全般相場急落に消されている。全般相場が落ち着けば見直されることが予想される。同社の山田英社長への取材を交えて株価の行方を展望した。
<Q>今回の海外での開発変更をマーケットの一部ではマイナスに受け取った向きもあるようです。
<山田社長>マイナスではありません。むしろ、プラスの話です。2019年の承認申請というゴールは全く変えていません。ゴールに向って一歩でも早く近づき、しかも、費用を5割ていど削減することが今回の変更の目的です。
<Q>これまでの海外での開発状況と今回の変更に至った経緯を教えてください。
<山田社長>2014年12月から重症虚血肢(糖尿病が原因で下肢切断に至る病変)を対象としたHGF遺伝子治療薬のグローバル第Ⅲ相臨床試験を実施しています。この試験は海外における承認申請を行うためのデータを取得することを目的に日本を除く北米、欧州など15カ国において約500例の被験者の登録を目指しているものです。しかし、被験者の登録ペースが想定よりも遅いことを米FDAとわれわれが認識を共有、新しい開発戦略に基づいた別の臨床試験を行う方針へ変更することを決定しました。
<Q>どのような内容ですか。
<山田社長>(1)重症虚血肢の主要な臨床症状である潰瘍と痛みの改善に変更します。これまでは、足の大切断、あるいは死亡という重度が対象でした、(2)試験の実施をアメリカ国内の施設に限定して行います。アメリカがもっとも重症虚血下肢治療の実績が豊富なためです。
<Q>これまで、実施の試験で安全性の問題は。
<山田社長>これまで実施してきた臨床試験においてHGF遺伝子治療薬が原因となる重大な安全性の問題は報告されていません。
<Q>新しい試験の開始はいつ頃になりますか。
<山田社長>新たな試験計画についてFDAと詰めの協議を終えたのちに開始します。それほど時間はかからないと思います。始まればスピードは速いと思います。
<Q>森下仁丹へのCIN治療ワクチン開発等許諾について概要をお願いします。
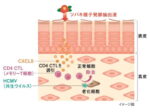
<山田社長>CIN治療ワクチンは、子宮頚がんの原因ウイルスであるヒトパピローマウイルスのたんぱく質に対する特異的な細胞性免疫を子宮頚部粘膜へ効率的に誘導します。これによって、子宮頚部の前がん病変を退縮、消失させます。経口投与で子宮頸がんへの移行を回避できる世界初のワクチンです。正式契約は年内の予定で、契約時に契約金、商業化時にロヤリティを受け取る内容です。
HGF遺伝子治療薬開発は、アメリカの有力100施設ていどとなるようで、これによってアメリカでの先行開発が進むことになる。進行中の日本での医師主導型の臨床研究と併せて注目されることになろう。全般相場さえ落ち着けばHGF遺伝子治療薬の開発進展と経費削減を評価するとみられる。値動きの軽い銘柄だけに大きく出直り、お預けとなっていた4ケタ乗せの可能性もありそうだ。
IR-Solution