- Home
- 新製品&新技術NOW
- ソレイジア・ファーマは開発品SP-02(新規抗がん剤) のアジア国際共同第II相臨床試験の解析結果を発表
ソレイジア・ファーマは開発品SP-02(新規抗がん剤) のアジア国際共同第II相臨床試験の解析結果を発表
- 2020/6/16 07:18
- 新製品&新技術NOW

◇主要評価項目を達成し、新たな安全性上の懸念は確認されず
ソレイジア・ファーマ<4597>(東マ)は、開発品SP-02(新規抗がん剤) の、再発又は難治性の末梢性T細胞リンパ腫(以下、「PTCL」)を対象としたアジア国際共同第II相臨床試験の解析結果を発表した。
解析結果によると、主要評価項目(SP-02抗腫瘍効果)を達成し、安全性においては、新たな安全性上の懸念は確認されなかったことから、承認申請の準備を開始することとなった。
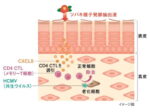
SP-02は、種々の血液がん及び固形がんの治療のために開発が進められてきた新規のミトコンドリア標的薬剤(有機ヒ素化合物)で、本試験は、再発又は難治性の PTCL患者を対象に、SP-02の単独投与時の有効性及び安全性を評価するために、国際多施設共同・単一群・非盲検・ 非無作為化試験として、日本、韓国、台湾及び香港にて実施された。
同社はSP-02の全世界権利を有しており、本開発品の事業化策として日本地域は Meiji Seikaファルマ株式会社と、また南米地域は hb Human BioScience SAS社と販売等にかかるライセ ンス契約を既に締結している。今後、米国、欧州等諸地域を対象としたライセンス権導出を積極的に展開する。
なお、本件による収益拡大、事業価値向上等への主な影響は長期に及ぶものと想定され、当期業績予想への影響はなく、その変更は行わない。